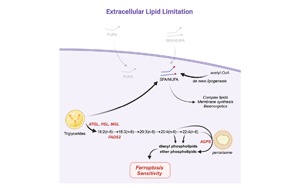
范安德?tīng)栄芯克茖W(xué)家研究發(fā)現(xiàn),切斷癌細(xì)胞獲得脂肪的途徑、限制癌細(xì)胞外脂質(zhì),可增加癌細(xì)胞對(duì)鐵死亡的敏感性,盡管可以氧化的細(xì)胞PUFAs水平降低。利用基于質(zhì)譜的脂質(zhì)組學(xué)和穩(wěn)定同位素脂肪酸標(biāo)記,作者對(duì)脂質(zhì)限制如何改變細(xì)胞脂質(zhì)代謝途徑活性進(jìn)行詳細(xì)研究
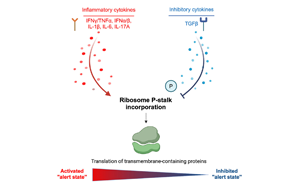
Cell:癌細(xì)胞通過(guò)改變核糖體來(lái)逃避免疫系統(tǒng)
荷蘭癌癥研究所的科學(xué)家們近日發(fā)現(xiàn),癌細(xì)胞可利用核糖體來(lái)增強(qiáng)它們的隱形能力,幫助它們躲避免疫系統(tǒng)。這項(xiàng)研究成果于2024年10月21日發(fā)表在《Cell》雜志上,有助于人們更深入了解免疫逃逸。
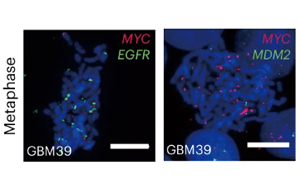
《Nature Biotechnology》新技術(shù)增強(qiáng)了對(duì)染色質(zhì)組織的認(rèn)識(shí)
加州大學(xué)圣地亞哥分校表觀基因組學(xué)中心(C4E)的研究人員開(kāi)發(fā)了一種名為“液滴Hi-C(Droplet Hi-C)”的新技術(shù),該技術(shù)使科學(xué)家能夠快速確定染色質(zhì)組織,即細(xì)胞內(nèi)遺傳物質(zhì)的排列。
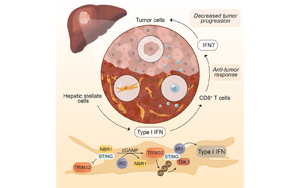
肝癌免疫治療成功的生物標(biāo)志物
研究發(fā)表在10月17日的《分子細(xì)胞》(Molecular Cell)雜志上,為一對(duì)名為p62和NBR1的蛋白質(zhì)提供了新的見(jiàn)解,以及它們?cè)谡{(diào)節(jié)肝星狀細(xì)胞干擾素反應(yīng)中的相反功能,肝星狀細(xì)胞是肝臟對(duì)抗腫瘤的關(guān)鍵免疫成分。該研究表明,這些特化細(xì)胞中高水平的免疫抑制NBR1可能會(huì)識(shí)別出不太可能對(duì)免疫療法產(chǎn)生反應(yīng)的患者。該研究還表明,在動(dòng)物模型中,降低nbr1的策略有助于縮小腫瘤,這為那些對(duì)免疫治療無(wú)反應(yīng)的患者提供了一種潛在的新治療方法。
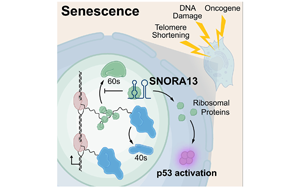
《Cell》一種small RNA有潛力逆轉(zhuǎn)衰老
發(fā)表在《Cell》雜志上的一篇文章中,科學(xué)家們把注意力集中在一種小核核RNAs (snoRNAs)上,這種RNA通過(guò)抑制核糖體的產(chǎn)生而使細(xì)胞停止分裂除了擴(kuò)大科學(xué)家對(duì)這類生物分子在細(xì)胞衰老中的作用的了解之外,這些發(fā)現(xiàn)還可以為設(shè)計(jì)新的核糖體疾病治療方法提供信息。
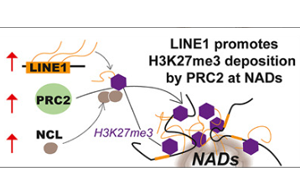
科學(xué)家揭示了“自私DNA”在人類早期發(fā)育中的關(guān)鍵作用
西奈健康中心的研究人員發(fā)現(xiàn),人類早期發(fā)育的一個(gè)關(guān)鍵轉(zhuǎn)變不是由我們自己的基因控制的,而是由一種叫做轉(zhuǎn)座子的DNA元素控制的,這種元素可以在基因組中移動(dòng)。他們發(fā)表在《發(fā)育細(xì)胞》(Developmental Cell)雜志上的研究表明,轉(zhuǎn)座因子對(duì)于確保人類胚胎細(xì)胞在早期正常發(fā)育(而不是回到過(guò)去)至關(guān)重要。研究人員專注于被稱為L(zhǎng)INE-1的轉(zhuǎn)座元素,即長(zhǎng)時(shí)間散布的核元素-1。
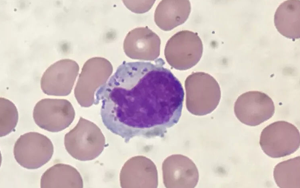
PNAS首次表明:人體組織中駐留在肺部的NK細(xì)胞在代謝方面與血液中循環(huán)的NK細(xì)胞不同
圣詹姆斯醫(yī)院都柏林三一學(xué)院的研究人員對(duì)一種以前基本上不為人知的、但至關(guān)重要的“自然殺手”(NK)免疫細(xì)胞的行為和代謝功能提供了重要的見(jiàn)解。他們的研究結(jié)果發(fā)表在今天(2024年10月10日星期四)的《美國(guó)國(guó)家科學(xué)院院刊》(PNAS)上,為進(jìn)一步探索NK細(xì)胞為一系列肺部疾病(包括慢性阻塞性肺疾病(COPD)、癌癥和結(jié)核病)的未來(lái)治療和療法的發(fā)展奠定了基礎(chǔ)。
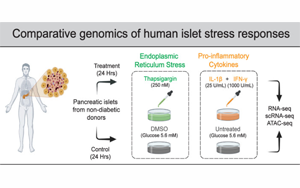
Cell Metabolism:糖尿病風(fēng)險(xiǎn)基因如何降低細(xì)胞對(duì)壓力的抵抗力
杰克遜實(shí)驗(yàn)室(JAX)的研究人員現(xiàn)在發(fā)現(xiàn),已知會(huì)增加一個(gè)人患糖尿病風(fēng)險(xiǎn)的DNA序列變化與胰腺細(xì)胞處理兩種不同分子壓力的能力有關(guān)。在有這些DNA變化的人身上,胰腺中產(chǎn)生胰島素的細(xì)胞在暴露于壓力和炎癥時(shí)可能更容易衰竭或死亡。
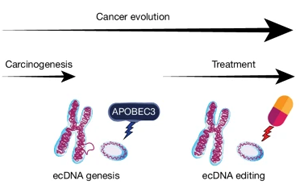
Nature:前所未有!新研究揭示了導(dǎo)致膀胱癌的突變和DNA結(jié)構(gòu)
威爾康奈爾醫(yī)學(xué)院和紐約基因組中心的研究人員領(lǐng)導(dǎo)的一項(xiàng)研究揭示了膀胱癌的起源和發(fā)展過(guò)程,這是前所未有的。研究人員發(fā)現(xiàn),使正常細(xì)胞和癌細(xì)胞的DNA發(fā)生突變的抗病毒酶是早期膀胱癌發(fā)展的關(guān)鍵促進(jìn)因素,而標(biāo)準(zhǔn)化療也是突變的一個(gè)有力來(lái)源。研究人員還發(fā)現(xiàn),腫瘤細(xì)胞中異常環(huán)狀DNA結(jié)構(gòu)中過(guò)度活躍的基因會(huì)導(dǎo)致膀胱癌對(duì)治療產(chǎn)生耐藥性。這些發(fā)現(xiàn)是對(duì)膀胱癌生物學(xué)的新見(jiàn)解,并為這種難以治療的癌癥提供了新的治療策略。