摘要:研究人員分析了轉移性腎癌患者的血樣,作為免疫治療抵抗研究的一部分。
UT西南醫學中心研究人員發現的一種蛋白質可能會導致對免疫檢查點抑制劑的耐藥性,這是一種廣泛用于治療癌癥的免疫療法。研究結果發表于Communications Medicine將糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)與治療后復發聯系起來,并表明它可能有助于腫瘤逃避轉移性腎細胞癌的免疫監視。
 圖1 對免疫檢查點療法產生獲得性耐藥性的機制由糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)信號級聯反應所引發
圖1 對免疫檢查點療法產生獲得性耐藥性的機制由糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)信號級聯反應所引發研究負責人說:“發現血清GPNMB作為獲得性耐藥性的預測因子和克服癌癥免疫治療耐藥性的潛在靶點,有助于進一步改善癌癥患者的預后?!逼つw病科UT Southwestern和哈羅德·西蒙斯綜合癌癥中心 Kiyoshi Ariizumi教授說。
Kiyoshi Ariizumi博士是猶他州西南大學皮膚科教授,也是哈羅德·C·西蒙斯綜合癌癥中心的成員。
檢查點抑制劑通過消除阻止免疫細胞識別和消除腫瘤的分子“剎車”,提高了許多晚期癌癥患者的生存率。然而,最初對這種免疫治療有反應的患者中,有一半以上在持續治療的幾個月到幾年內,由于獲得性耐藥性,最終復發。
為了更好地了解這種耐藥性是如何形成的,UT西南大學的研究人員分析了39名接受免疫檢查點抑制劑治療的轉移性腎癌患者的腫瘤和血液樣本。在最初反應積極的患者中,28%的患者在兩年內產生了耐藥性,與血液中GPNMB水平的升高相一致。通過比較治療前和疾病進展后收集的樣本,該團隊調查了可能導致復發的分子變化。
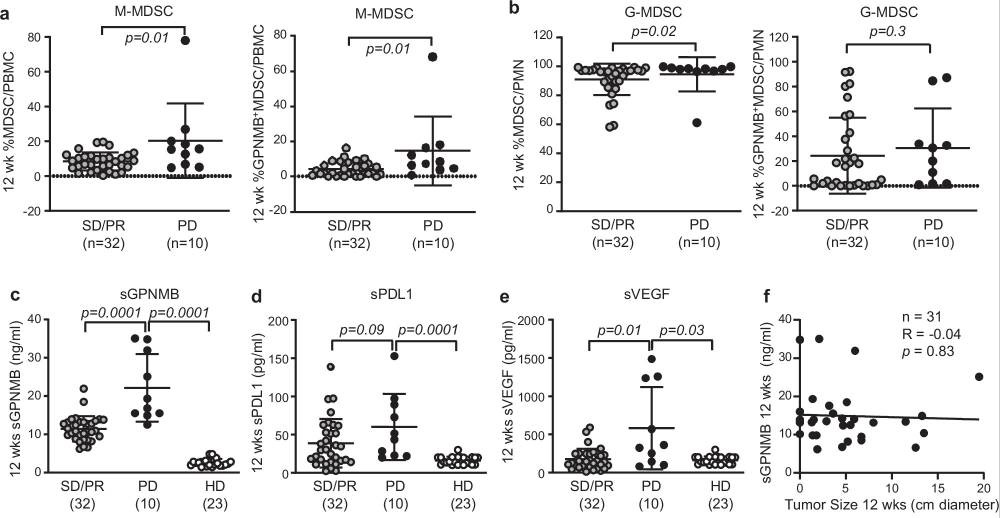
圖2 血液中可溶性糖蛋白非轉移性黑色素瘤蛋白B(sGPNMB)水平升高與免疫檢查點抑制劑(ICI)治療后12周時的腫瘤進展顯著相關
另一方面,在細胞應激期間,核糖體活動通常會減少,因此可供發生碰撞的核糖體數量減少。因此,含有m6A的mRNA得以積累并轉化為應激反應蛋白。
Jaffrey博士說:“m6A途徑通常有助于抑制細胞的應激反應,但我們知道在細胞應激時一定有一個開關將其關閉,而核糖體是這個開關的關鍵要素?!?/div> 圖1 對免疫檢查點療法產生獲得性耐藥性的機制由糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)信號級聯反應所引發
圖1 對免疫檢查點療法產生獲得性耐藥性的機制由糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)信號級聯反應所引發
圖2 血液中可溶性糖蛋白非轉移性黑色素瘤蛋白B(sGPNMB)水平升高與免疫檢查點抑制劑(ICI)治療后12周時的腫瘤進展顯著相關
這項發現可能對癌癥治療具有啟示意義。新興的抗m6A療法通過抑制催化m6A在mRNA上形成的酶METTL3,正在進行臨床試驗。這項研究提出了這些藥物可能通過誘導應激反應蛋白的表達來發揮作用的可能性,而應激反應蛋白已知可以抑制某些癌細胞的生長。
Jaffrey博士說:“我們的新發現為預測哪些類型的癌癥將對應METTL3抑制劑提供了策略,這可以幫助我們識別出將對該療法反應最佳的患者?!?/div>
參考資料
[1] Acquired resistance to immune checkpoint therapy is caused by glycoprotein non-metastatic melanoma protein B signal cascade
摘要:研究人員分析了轉移性腎癌患者的血樣,作為免疫治療抵抗研究的一部分。
UT西南醫學中心研究人員發現的一種蛋白質可能會導致對免疫檢查點抑制劑的耐藥性,這是一種廣泛用于治療癌癥的免疫療法。研究結果發表于Communications Medicine將糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)與治療后復發聯系起來,并表明它可能有助于腫瘤逃避轉移性腎細胞癌的免疫監視。
 圖1 對免疫檢查點療法產生獲得性耐藥性的機制由糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)信號級聯反應所引發
圖1 對免疫檢查點療法產生獲得性耐藥性的機制由糖蛋白非轉移性黑色素瘤蛋白B(GPNMB)信號級聯反應所引發研究負責人說:“發現血清GPNMB作為獲得性耐藥性的預測因子和克服癌癥免疫治療耐藥性的潛在靶點,有助于進一步改善癌癥患者的預后?!逼つw病科UT Southwestern和哈羅德·西蒙斯綜合癌癥中心 Kiyoshi Ariizumi教授說。
Kiyoshi Ariizumi博士是猶他州西南大學皮膚科教授,也是哈羅德·C·西蒙斯綜合癌癥中心的成員。
檢查點抑制劑通過消除阻止免疫細胞識別和消除腫瘤的分子“剎車”,提高了許多晚期癌癥患者的生存率。然而,最初對這種免疫治療有反應的患者中,有一半以上在持續治療的幾個月到幾年內,由于獲得性耐藥性,最終復發。
為了更好地了解這種耐藥性是如何形成的,UT西南大學的研究人員分析了39名接受免疫檢查點抑制劑治療的轉移性腎癌患者的腫瘤和血液樣本。在最初反應積極的患者中,28%的患者在兩年內產生了耐藥性,與血液中GPNMB水平的升高相一致。通過比較治療前和疾病進展后收集的樣本,該團隊調查了可能導致復發的分子變化。

圖2 血液中可溶性糖蛋白非轉移性黑色素瘤蛋白B(sGPNMB)水平升高與免疫檢查點抑制劑(ICI)治療后12周時的腫瘤進展顯著相關
另一方面,在細胞應激期間,核糖體活動通常會減少,因此可供發生碰撞的核糖體數量減少。因此,含有m6A的mRNA得以積累并轉化為應激反應蛋白。
Jaffrey博士說:“m6A途徑通常有助于抑制細胞的應激反應,但我們知道在細胞應激時一定有一個開關將其關閉,而核糖體是這個開關的關鍵要素。”
這項發現可能對癌癥治療具有啟示意義。新興的抗m6A療法通過抑制催化m6A在mRNA上形成的酶METTL3,正在進行臨床試驗。這項研究提出了這些藥物可能通過誘導應激反應蛋白的表達來發揮作用的可能性,而應激反應蛋白已知可以抑制某些癌細胞的生長。
Jaffrey博士說:“我們的新發現為預測哪些類型的癌癥將對應METTL3抑制劑提供了策略,這可以幫助我們識別出將對該療法反應最佳的患者?!?/div>
參考資料
[1] Acquired resistance to immune checkpoint therapy is caused by glycoprotein non-metastatic melanoma protein B signal cascade



