摘要:新研究表明,一種特殊的脂質(zhì)類型實際上對癌癥免疫逃避至關(guān)重要。
癌細胞很少悄無聲息地開始。恰恰相反,它們通過在細胞膜上植入化學(xué)紅旗來向免疫系統(tǒng)宣布自己的存在。一旦受到警告,身體的防御系統(tǒng)就會迅速出擊,在流氓細胞造成更大傷害之前將其摧毀。這個早期預(yù)警系統(tǒng)的核心是脂質(zhì),這是一種脂肪化合物,以前癌癥生物學(xué)家認為它主要是腫瘤生長的燃料來源。
但現(xiàn)在,《Nature》雜志上的一項新研究表明,一種特殊的脂質(zhì)類型實際上對癌癥免疫逃避至關(guān)重要。以至于某些癌細胞沒有它就無法增殖。這些發(fā)現(xiàn)證實了長期以來的懷疑,即這種脂質(zhì)不僅是癌癥生物學(xué)中的關(guān)鍵角色(因此也是關(guān)鍵的藥物靶點),而且還證明了現(xiàn)有的FDA批準的旨在抑制脂質(zhì)產(chǎn)生的藥物可以激發(fā)免疫系統(tǒng)對抗癌癥。Lime Therapeutics的研究第一作者和科學(xué)家Mariluz Soula說:“癌細胞正在改變這種脂質(zhì)代謝的方式,這反過來又扭曲了惡性細胞通常產(chǎn)生的“吃我”信號。這描繪了脂質(zhì)在癌癥生長中所起作用的一幅非常不同的畫面。”

圖1 糖鞘脂合成介導(dǎo)KRAS驅(qū)動的癌癥免疫逃避
脂質(zhì)和癌癥之間的神秘聯(lián)系
科學(xué)家們早就知道癌細胞會改變脂質(zhì)代謝,但人們通常認為癌細胞是在吞噬這些脂質(zhì)以獲取能量。消耗脂肪分子,幫助腫瘤生長和擴散,遠遠超過健康細胞。
“我們從文獻中知道,血脂水平升高與癌癥生長和轉(zhuǎn)移的嚴重程度有關(guān),但不清楚是如何關(guān)聯(lián)的,”Soula說。Birsoy實驗室與Gabriel D. Victoria的實驗室合作,開始通過篩選參與這一過程的基因來回答這個問題。然后,他們將一系列缺失不同基因的癌細胞植入有免疫系統(tǒng)和沒有免疫系統(tǒng)的小鼠體內(nèi)。從而揭示了癌癥離不開哪些脂質(zhì)。
結(jié)果就是所謂的“鞘脂”。鞘脂是由德國化學(xué)家約翰·路德維希·威廉·圖迪丘姆在19世紀末發(fā)現(xiàn)的,由于其令人費解的結(jié)構(gòu)和功能,鞘脂以希臘神話中神秘的獅身人面像命名。兩個世紀后,鞘脂不再那么神秘了。“我們知道鞘脂并不是真正用于能量,”Soula說。“它們主要存在于細胞膜中,為信號蛋白提供支架。”
這一發(fā)現(xiàn)提出了一個有趣的可能性。癌細胞中的脂質(zhì)代謝真的只是饑餓細胞試圖消耗更多能量的過程嗎?或者它是癌細胞巧妙地操縱細胞信號并躲避免疫系統(tǒng)的關(guān)鍵部分?
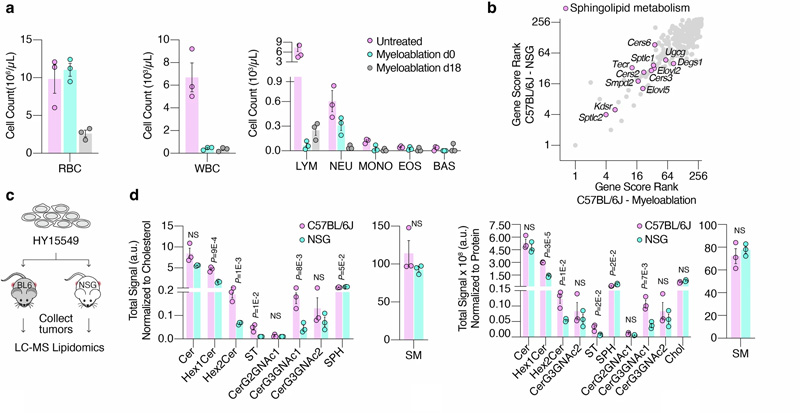
圖2 癌癥細胞鞘脂的可用性介導(dǎo)免疫逃避
為了測試鞘脂是如何推動癌癥生長的,研究小組轉(zhuǎn)向了一種FDA批準的治療戈謝病的藥物,戈謝病是一種以分解脂質(zhì)能力受損為特征的遺傳性疾病。該藥物基本上阻斷了鞘糖脂的合成,研究小組發(fā)現(xiàn),在胰腺癌、肺癌和結(jié)直腸癌模型中,這種藥物會損害腫瘤的生長。
他們還發(fā)現(xiàn),鞘糖脂的消耗阻止了“脂質(zhì)納米結(jié)構(gòu)域”的形成,這種結(jié)構(gòu)域?qū)⑿盘柗肿泳奂谀ど希绊懠毎砻娴氖荏w,使它們對免疫反應(yīng)更敏感。這些發(fā)現(xiàn)表明,癌細胞囤積鞘糖脂是為了掩蓋炎癥信號,而破壞鞘糖脂的產(chǎn)生會使癌細胞容易受到免疫系統(tǒng)的攻擊。
“每個人都認為升高的脂質(zhì)水平是癌細胞消耗的能量來源,”Soula說。“我們發(fā)現(xiàn)它要微妙得多。脂質(zhì)不僅是燃料,也是癌細胞的一種保護機制,可以調(diào)節(jié)癌細胞與免疫系統(tǒng)的溝通方式。”
未來的工作將確定這是否適用于多種癌癥。該團隊測試了多種類型,但發(fā)現(xiàn)這種機制在依賴KRAS的癌癥(以驅(qū)動它們的突變致癌基因命名)中起作用。盡管如此,考慮到許多依賴KRAS的癌癥(如胰腺癌)的侵襲性,初步結(jié)果可能會產(chǎn)生重大的臨床影響。基于他們的發(fā)現(xiàn),研究小組建議,通過藥物和飲食干預(yù)來抑制鞘脂的產(chǎn)生,可能有助于提高現(xiàn)有免疫療法的療效。
“飲食可能會影響癌癥生物學(xué)的許多方面,”Birsoy說。“我們相信,調(diào)節(jié)膳食脂質(zhì)可能是一種有趣的途徑,可以瞄準癌細胞逃避免疫細胞的能力。”
參考資料
[1] Glycosphingolipid synthesis mediates immune evasion in KRAS-driven cancer
摘要:新研究表明,一種特殊的脂質(zhì)類型實際上對癌癥免疫逃避至關(guān)重要。
癌細胞很少悄無聲息地開始。恰恰相反,它們通過在細胞膜上植入化學(xué)紅旗來向免疫系統(tǒng)宣布自己的存在。一旦受到警告,身體的防御系統(tǒng)就會迅速出擊,在流氓細胞造成更大傷害之前將其摧毀。這個早期預(yù)警系統(tǒng)的核心是脂質(zhì),這是一種脂肪化合物,以前癌癥生物學(xué)家認為它主要是腫瘤生長的燃料來源。
但現(xiàn)在,《Nature》雜志上的一項新研究表明,一種特殊的脂質(zhì)類型實際上對癌癥免疫逃避至關(guān)重要。以至于某些癌細胞沒有它就無法增殖。這些發(fā)現(xiàn)證實了長期以來的懷疑,即這種脂質(zhì)不僅是癌癥生物學(xué)中的關(guān)鍵角色(因此也是關(guān)鍵的藥物靶點),而且還證明了現(xiàn)有的FDA批準的旨在抑制脂質(zhì)產(chǎn)生的藥物可以激發(fā)免疫系統(tǒng)對抗癌癥。Lime Therapeutics的研究第一作者和科學(xué)家Mariluz Soula說:“癌細胞正在改變這種脂質(zhì)代謝的方式,這反過來又扭曲了惡性細胞通常產(chǎn)生的“吃我”信號。這描繪了脂質(zhì)在癌癥生長中所起作用的一幅非常不同的畫面。”

圖1 糖鞘脂合成介導(dǎo)KRAS驅(qū)動的癌癥免疫逃避
脂質(zhì)和癌癥之間的神秘聯(lián)系
科學(xué)家們早就知道癌細胞會改變脂質(zhì)代謝,但人們通常認為癌細胞是在吞噬這些脂質(zhì)以獲取能量。消耗脂肪分子,幫助腫瘤生長和擴散,遠遠超過健康細胞。
“我們從文獻中知道,血脂水平升高與癌癥生長和轉(zhuǎn)移的嚴重程度有關(guān),但不清楚是如何關(guān)聯(lián)的,”Soula說。Birsoy實驗室與Gabriel D. Victoria的實驗室合作,開始通過篩選參與這一過程的基因來回答這個問題。然后,他們將一系列缺失不同基因的癌細胞植入有免疫系統(tǒng)和沒有免疫系統(tǒng)的小鼠體內(nèi)。從而揭示了癌癥離不開哪些脂質(zhì)。
結(jié)果就是所謂的“鞘脂”。鞘脂是由德國化學(xué)家約翰·路德維希·威廉·圖迪丘姆在19世紀末發(fā)現(xiàn)的,由于其令人費解的結(jié)構(gòu)和功能,鞘脂以希臘神話中神秘的獅身人面像命名。兩個世紀后,鞘脂不再那么神秘了。“我們知道鞘脂并不是真正用于能量,”Soula說。“它們主要存在于細胞膜中,為信號蛋白提供支架。”
這一發(fā)現(xiàn)提出了一個有趣的可能性。癌細胞中的脂質(zhì)代謝真的只是饑餓細胞試圖消耗更多能量的過程嗎?或者它是癌細胞巧妙地操縱細胞信號并躲避免疫系統(tǒng)的關(guān)鍵部分?

圖2 癌癥細胞鞘脂的可用性介導(dǎo)免疫逃避
為了測試鞘脂是如何推動癌癥生長的,研究小組轉(zhuǎn)向了一種FDA批準的治療戈謝病的藥物,戈謝病是一種以分解脂質(zhì)能力受損為特征的遺傳性疾病。該藥物基本上阻斷了鞘糖脂的合成,研究小組發(fā)現(xiàn),在胰腺癌、肺癌和結(jié)直腸癌模型中,這種藥物會損害腫瘤的生長。
他們還發(fā)現(xiàn),鞘糖脂的消耗阻止了“脂質(zhì)納米結(jié)構(gòu)域”的形成,這種結(jié)構(gòu)域?qū)⑿盘柗肿泳奂谀ど希绊懠毎砻娴氖荏w,使它們對免疫反應(yīng)更敏感。這些發(fā)現(xiàn)表明,癌細胞囤積鞘糖脂是為了掩蓋炎癥信號,而破壞鞘糖脂的產(chǎn)生會使癌細胞容易受到免疫系統(tǒng)的攻擊。
“每個人都認為升高的脂質(zhì)水平是癌細胞消耗的能量來源,”Soula說。“我們發(fā)現(xiàn)它要微妙得多。脂質(zhì)不僅是燃料,也是癌細胞的一種保護機制,可以調(diào)節(jié)癌細胞與免疫系統(tǒng)的溝通方式。”
未來的工作將確定這是否適用于多種癌癥。該團隊測試了多種類型,但發(fā)現(xiàn)這種機制在依賴KRAS的癌癥(以驅(qū)動它們的突變致癌基因命名)中起作用。盡管如此,考慮到許多依賴KRAS的癌癥(如胰腺癌)的侵襲性,初步結(jié)果可能會產(chǎn)生重大的臨床影響。基于他們的發(fā)現(xiàn),研究小組建議,通過藥物和飲食干預(yù)來抑制鞘脂的產(chǎn)生,可能有助于提高現(xiàn)有免疫療法的療效。
“飲食可能會影響癌癥生物學(xué)的許多方面,”Birsoy說。“我們相信,調(diào)節(jié)膳食脂質(zhì)可能是一種有趣的途徑,可以瞄準癌細胞逃避免疫細胞的能力。”
參考資料
[1] Glycosphingolipid synthesis mediates immune evasion in KRAS-driven cancer



